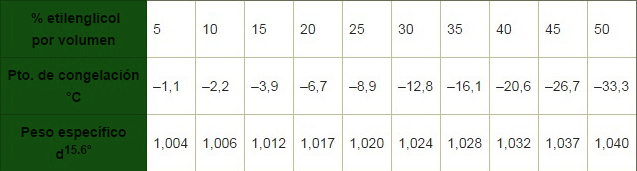
Tabla de puntos de congelación ETG-Agua

De venta libre
Es tóxico.
Fórmula química
HOCH2CH2OH
CAS: 107-21-1
Fórmula: HOCH2CH2OH
Masa molecular: 62.1
Punto de ebullición: 197°C
Punto de fusión: -13°C
Densidad relativa (agua = 1): 1.1
Solubilidad en agua: miscible
Presión de vapor, Pa a 20°C: 6.5
Densidad relativa de vapor (aire = 1): 2.1
Densidad relativa de la mezcla vapor/aire a 20°C (aire = 1): 1.00
Punto de inflamación: 111.11°C c.c., 115°C c.a.
Temperatura de autoignición: 398°C
Límites de explosividad, % en volumen en el aire: 3.2-15.3
Coeficiente de reparto octanol/agua como log Pow: -1.36
Viscosidad: 21 mPa/s a 20°C
ETILENGLICOL
1,2-Etanodiol,
1,2-Dihidroxietano,
2-Hidroxietanol,
Glicol,
Monoetilenglicol
El etilenglicol, etanodiol, glicol de etileno, glicol o dihidroxido de etileno, es un compuesto químico orgánico que pertenece al grupo de los dioles. Es un líquido transparente, incoloro, ligeramente viscoso como el almíbar.
A temperatura ambiente es poco volátil, pero puede existir en el aire en forma de vapor. Se fabrica a partir de la hidratación del óxido de etileno.
Se utiliza como anticongelante en los circuitos de refrigeración de motores de combustión interna, como difusor del calor, mezclado con agua para los procedimientos de deshielo y antihielo de los aviones comerciales.
El etilenglicol se utiliza principalmente como medio para la transferencia de calor por convección en automóviles y computadoras refrigeradas por líquido..
Se usa a menudo en sistemas de aire acondicionado de agua fría que colocan el enfriador o las unidades de tratamiento de aire en el exterior, o en sistemas que necesitan enfriarse por debajo de la temperatura de congelación del agua.
En los sistemas de calefacción / refrigeración geotérmicos, el etilenglicol es el fluido que transporta el calor por medio de una bomba de calor geotérmica. Extrae energía de la fuente (lago, océano, pozo) o disipa el calor hacia el disipador, dependiendo de si el sistema se usa para calentar o enfriar.
El etilenglicol puro tiene una capacidad calorífica específica de aproximadamente la mitad de la del agua. Entonces, mientras que el etilenglicol protege contra la congelación y aumenta el punto de ebullición, reduce la capacidad calorífica específica de las mezclas de agua en relación con el agua pura.
Una mezcla de masa 1: 1 tiene una capacidad calorífica específica de aproximadamente 3140 J / (kg ° C) (0,75 BTU / (lb ° F)), tres cuartas partes de la del agua pura, lo que significa que se requiere un caudal más alto en el mismo sistema son comparaciones con el agua.
La mezcla de etilenglicol con agua proporciona beneficios adicionales para las soluciones refrigerantes y anticongelantes, como prevenir la corrosión y la degradación del ácido, así como inhibir el crecimiento de la mayoría de los microbios y hongos.
El etilenglicol puro se congela a aproximadamente -12 ° C (10,4 ° F), pero cuando se mezcla con agua, la mezcla se congela a una temperatura más baja.
Una mezcla de 60% de etilenglicol y 40% de agua se congela a -45 ° C (-49 ° F).
El dietilenglicol se comporta de la misma manera.
La depresión del punto de congelación de algunas mezclas puede explicarse como una propiedad coligativa de las soluciones, pero en mezclas altamente concentradas como el ejemplo, se esperan desviaciones del comportamiento ideal de la solución debido a la influencia de fuerzas intermoleculares.
Existe una diferencia en la proporción de mezcla dependiendo de si es etilenglicol o propilenglicol.
Para etilenglicol, las proporciones de mezcla son típicamente 30/70 y 35/65, mientras que las proporciones de mezcla de propilenglicol son típicamente 35/65 y 40/60. Es importante que la mezcla sea resistente a las heladas a la temperatura de funcionamiento más baja.
Debido a las bajas temperaturas de congelación, el etilenglicol se utiliza como líquido descongelante para parabrisas y aviones, como anticongelante en motores de automóviles y como parte de mezclas de vidriado (anticristalización) para la conservación de tejidos y órganos biológicos a bajas temperaturas.
La mezcla de etilenglicol y agua también puede denominarse químicamente concentrado / compuesto / mezcla / solución de glicol.
El uso de etilenglicol no solo reduce el punto de congelación de las mezclas acuosas, sino que también aumenta su punto de ebullición. Esto tiene el efecto de ampliar el rango de temperatura de funcionamiento para los fluidos de transferencia de calor en ambos extremos de la escala de temperatura.
El aumento de la temperatura de ebullición se debe al etilenglicol puro con un punto de ebullición mucho más alto y una presión de vapor más baja que el agua pura, como es típico para la mayoría de las mezclas binarias de líquidos volátiles.
En la industria del plástico, el etilenglicol es un precursor importante de las fibras y resinas de poliéster. El tereftalato de polietileno, que se utiliza para fabricar botellas de plástico para refrescos, se prepara a partir de etilenglicol.
El etilenglicol se utiliza en la industria del gas natural para eliminar el vapor de agua del gas natural para su procesamiento posterior, de la misma manera que el trietilenglicol (TEG).
Debido a su alto punto de ebullición y afinidad por el agua, el etilenglicol es un agente de secado útil. El etilenglicol se usa ampliamente para inhibir la formación de clatratos (hidratos) de gas natural en tuberías multifase largas que transportan gas natural desde campos de gas remotos hasta una planta de procesamiento de gas.
El etilenglicol puede extraerse del gas natural y reutilizarse como inhibidor después de un tratamiento de purificación que elimina el agua y las sales inorgánicas.
El gas natural se deshidrata con etilenglicol. En esta aplicación, el etilenglicol fluye hacia abajo desde la parte superior de una torre y encuentra una mezcla ascendente de vapor de agua y gases de hidrocarburos.
El gas seco sale de la parte superior de la torre. El glicol y el agua se separan y el glicol se recicla. En lugar de eliminar el agua, también se puede utilizar etilenglicol para reducir la temperatura a la que se forman los hidratos. La pureza del glicol usado para la supresión de hidratos (monoetilenglicol) es típicamente de aproximadamente el 80%, mientras que la pureza del glicol usado para la deshidratación (trietilenglicol) es típicamente del 95 a más del 99%. Además, la velocidad de inyección de supresión de hidratos es mucho más lenta que la velocidad de circulación en una torre de deshidratación de glicol.
Los usos menores del etilenglicol incluyen;

Recibir asesoramiento técnico o comercial, acerca de este producto.